Hlavný rozdiel: Iónová väzba je chemická väzba medzi dvomi odlišnými (tj kovovými a nekovovými) atómami, v ktorých jeden atóm odovzdá elektrón druhému. Kovalentná väzba je ďalšou silnou chemickou väzbou. Prebieha podobné atómy (tj dva nekovy). V kovalentnej väzbe sa dva atómy stretávajú, aby zdieľali elektrón, namiesto toho, aby atóm odoberal elektrón od druhého.
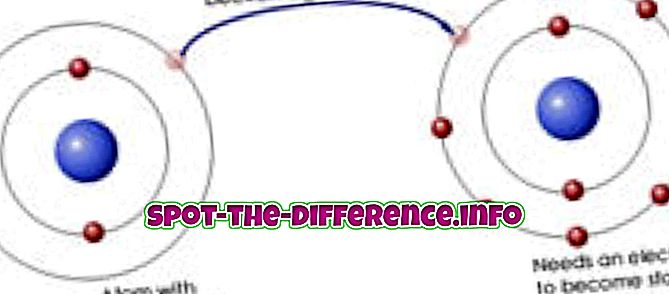
Iónová väzba je chemická väzba medzi dvomi odlišnými (tj kovovými a nekovovými) atómami, v ktorých jeden atóm odovzdá elektrón druhému. Preto sa obidva atómy stanú iónmi, pretože jeden atóm má jeden elektrón menej, druhý má extra. Kovový ión, ktorý stratil elektrón, má pozitívny náboj. Nekovový ión, ktorý získal elektrón, má záporný náboj. Ako protiklady priťahujú, tieto ióny sú silne priťahované jeden k druhému, tak silne, že sa spájajú.
Iónové zlúčeniny sú zvyčajne vo forme tuhých látok, tj solí. Sú vysoko rozpustné vo vode a majú vysokú teplotu topenia. Keď sú vo vode, majú tiež vysokú elektrickú vodivosť.

Kovalentné viazanie zahŕňa mnoho druhov interakcií vrátane väzby σ, väzbu π, spojenie kovu s kovom, agostické interakcie a trojcentrové dvoj-elektrónové väzby. Keď atóm má vo svojom vonkajšom plášti elektrón a iné atómy vyžadujú elektrón na vyplnenie jeho vonkajšieho plášťa, obidva atómy sa spolu zdieľajú s elektrónom. Preto obe atómy majú úplnú vonkajšiu škrupinu a zodpovedajúcu stabilnú elektronickú konfiguráciu.
Chemické väzby sú vytvorené tak, že atóm môže mať celú vonkajšiu škrupinu, pretože úplná vonkajšia škrupina znamená stabilnú elektronickú konfiguráciu. V iónovej väzbe, keď atóm kovu má vo svojom vonkajšom plášti jediný elektrón a nekovový potrebuje elektrón na vyplnenie jeho vonkajšieho plášťa, atóm kovu dáva svoj elektrón nekovu. Podobne v kovalentnej väzbe spoločne zdieľajú elektrón.
Ionic Bond | Kovalentná väzba | |
definícia | Chemická väzba medzi dvomi rôznymi atómami, v ktorých atóm uvoľňuje elektrón do druhého. | Kovalentná väzba je chemická väzba, ktorá zahŕňa zdieľanie elektrónov medzi dvomi podobnými atómami. |
výskyt | Kov a nekov | Dva nekovy |
polarita | vysoký | nízky |
Tvar molekuly | Žiadny definitívny tvar, mriežkové štruktúry | Určený tvar |
Elektrická vodivosť | vysoký | Zvyčajne žiadny |
Tepelná vodivosť | vysoký | Zvyčajne nízka |
Bod topenia látky | Rôzne, ale zvyčajne vyššie ako kovalentné zlúčeniny | Rôzne, ale zvyčajne nižšie ako iónové zlúčeniny |
Bod varu látky | vysoký | Rôzne, ale zvyčajne nižšie ako iónové zlúčeniny |
Rozpustnosť vo vode | vysoký | Rôzne, ale zvyčajne nižšie ako iónové zlúčeniny |
Stav látky pri izbovej teplote | Zvyčajne pevný | Tuhá látka, kvapalina, plyn |