Hlavný rozdiel: Atómy sú základnými jednotkami, z ktorých je všetka záležitosť. Atómov rôznych prvkov sa spájajú, aby vytvorili molekuly. To sa deje prostredníctvom chemickej reakcie. Molekula je najmenšie množstvo chemickej látky, ktorá môže existovať. V podstate zlúčenina je typ molekuly. Molekula môže byť tvorená dvoma alebo viacerými atómami rovnakého prvku alebo dvomi alebo viacerými atómami rôznych prvkov. Avšak zlúčeniny sú molekuly, ktoré sú tvorené atómami rôznych molekúl.
Prvok je čistá chemická látka, ktorá má jeden alebo jeden typ atómu, ktorý sa vyznačuje jeho atómovým číslom. Atómové číslo je odvodené od počtu protónov prítomných v jadre prvku. Existuje celkovo 118 identifikovaných prvkov, rozdelených medzi kovy, metaloidy a nekovy. Každý prvok má vlastnú sadu vlastností. Väčšina prvkov je k dispozícii na zemi, zatiaľ čo niektoré boli umelo vytvorené prostredníctvom jadrových reakcií. Prvok je už v najstaršej podobe a nemôže byť ďalej rozdelený. Všetky prvky sa nachádzajú v periodickej tabuľke, ktorá je uvedená podľa atómového čísla.
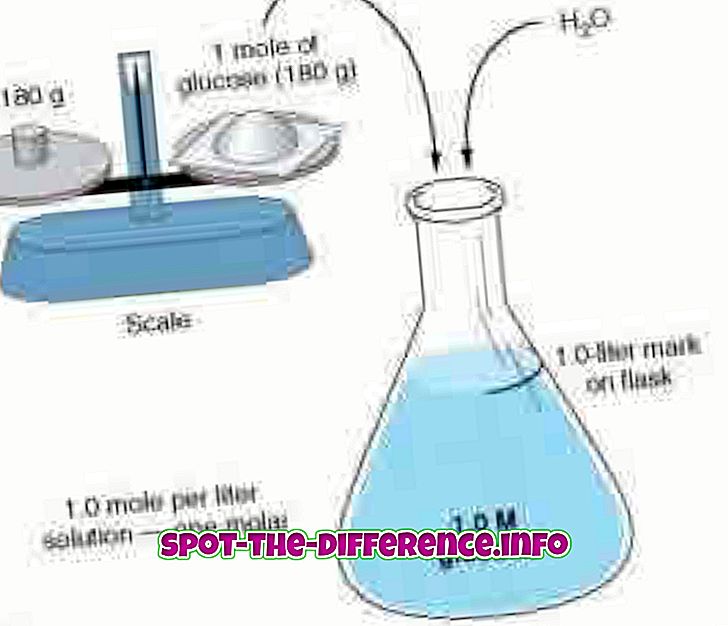
Atómov rôznych prvkov sa spájajú, aby vytvorili molekuly. To sa deje prostredníctvom chemickej reakcie. Napríklad: dva vodíkové atómy a jeden atóm kyslíka sa spoja, aby sa vytvorila molekula vody.
Molekula je najmenšie množstvo chemickej látky, ktorá môže existovať. Ako najmenšie množstvo vody môže byť molekula vody alebo H20. Vyrába sa z rôznych atómov dohromady; preto sa môže oddeliť späť do rôznych atómov.
Molekula môže mať veľmi odlišné vlastnosti od prvkov, z ktorých je vyrobená. Napríklad: voda sa správa veľmi odlišne ako kyslík alebo vodík, hoci je zložená z dvoch atómov vodíka a jedného atómu kyslíka.
Navyše atóm nemôže existovať nezávisle v prírode bez toho, aby na niečo viazal. Nikdy nenájdeme len jediný atóm kyslíka alebo jediný atóm uhlíka. Vždy je spojená s niečím, ako je O2 (kyslík) alebo CO2 (oxid uhličitý). Keď je molekula väzená do molekuly, môže existovať nezávisle od jej povahy, a preto môžeme vždy nájsť molekulu kyslíka, molekulu oxidu uhličitého, molekulu vody (H2O) atď.

Molekuly vždy majú tendenciu sa združovať, ich formovanie závisí od ich stavu. Ako v plynnom stave, molekuly majú tendenciu jednoducho lietať. V kvapalnom stave majú molekuly tendenciu byť voľne zoskupené tak, aby sa ešte mohli pohybovať. Zatiaľ čo v tuhom stave sú molekuly tesne zhromaždené a môžu vibrovať len.
Molekuly sú zvyčajne zastúpené v molekulárnom vzorci. Napríklad: O2, H2O, CO2, C6H12O6 (cukor). Molekulový vzorec je názov prvku, po ktorom nasleduje počet atómov tohto prvku v molekule.
V podstate zlúčenina je typ molekuly. Molekula môže byť tvorená dvoma alebo viacerými atómami rovnakého prvku alebo dvomi alebo viacerými atómami rôznych prvkov. Avšak zlúčeniny sú molekuly, ktoré sú tvorené atómami rôznych prvkov. Preto možno povedať, že všetky zlúčeniny sú molekuly, avšak nie všetky molekuly sú zlúčeniny.
Preto sú všetky molekuly vodík (H2), kyslík (02), dusík (N2), voda (H2O), oxid uhličitý (CO2) a metán (CH4). Avšak iba voda (H2O), oxid uhličitý (CO2) a metán (CH4) sú zlúčeniny, ostatné nie sú.