Hlavný rozdiel: Usporiadanie atómov v molekule pomáha určiť jej polaritu. Molekula sa považuje za polárnu, ak má pozitívny a záporný náboj. Nepolárna molekula je molekula s nižším nábojom.
V chémii sa polarita vzťahuje na oddelenie elektrických nábojov molekuly alebo jej chemickej skupiny, ktorá má elektrický dipól alebo viacpólový moment. Polárne molekuly interagujú prostredníctvom intermolekulárnych väzieb a vodíkových väzieb. Molekulárna polarita závisí od rozdielu v elektronegativite medzi atómami v molekule. Polarita tiež určuje množstvo fyzikálnych vlastností, ako je povrchové napätie, teploty topenia a varu a rozpustnosť.
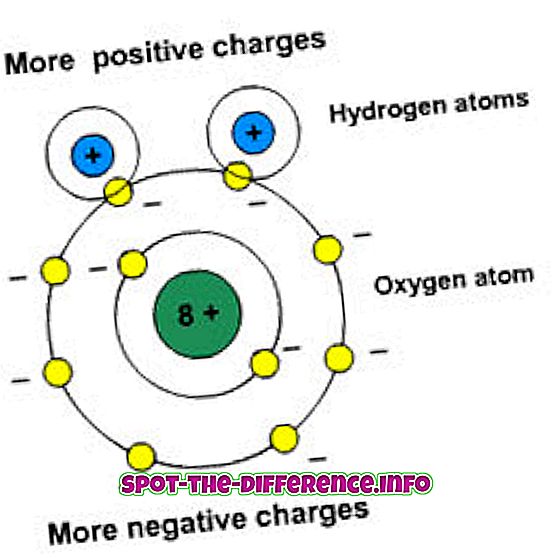
Polarita znamená oddelenie nábojov. Tieto molekuly majú dipólový moment. Dipólový moment meria polaritu väzby. Polárne látky interagujú s inými polárnymi prvkami.

Nepolárna molekula nemá dostatok náboja. Nepolárne molekuly sú distribuované spôsobom symetrie a na nich nemajú veľký počet elektrických nábojov. Ak dva atomy alebo dva rovnaké atómy majú medzi sebou rovnakú elektrónovú väzbu, atómy vytiahnu elektrónový pár. Toto ťahanie im pomáha zdieľať elektróny a tento druh zdieľania väzieb medzi molekulami je známy ako nepolárne kovalentné väzby.
Porovnanie medzi polárnou a nepolárnou:
polárne | Non-Polar | |
definícia | Polárne látky majú kladný a záporný náboj na atóme. | Nepolárne látky nemajú veľké náboje na pripevnenom atóme. |
pohyb | Majú elektrický dipólový pohyb. | Nemajú žiadne dipólové pohyby. |
Oddeľovanie nabíjania | Oddeľuje sa náboj. | Neexistuje žiadne oddelenie poplatkov. |
Interakcia | Spolupracujú s inými polárnymi látkami. | Neinteragujú s inými polárnymi látkami. |
príklad | Voda, alkohol a síra. | Oil. |