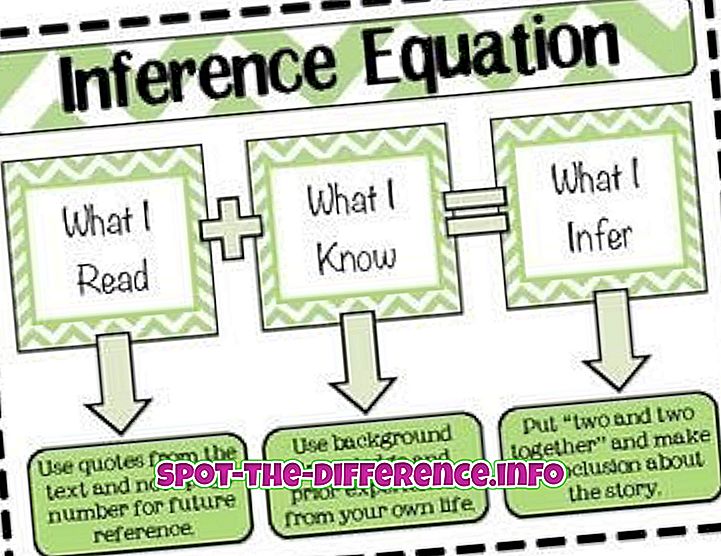
Kľúčový rozdiel: Absorpcia je hromadný fenomén, pri ktorom absorbent úplne preniká do tela pevného alebo kvapalného, čím vzniká zlúčenina alebo roztok. Na druhej strane adsorpcia je povrchový jav, v ktorom sa molekuly adsorbátu koncentrujú len na povrchu adsorbentu.
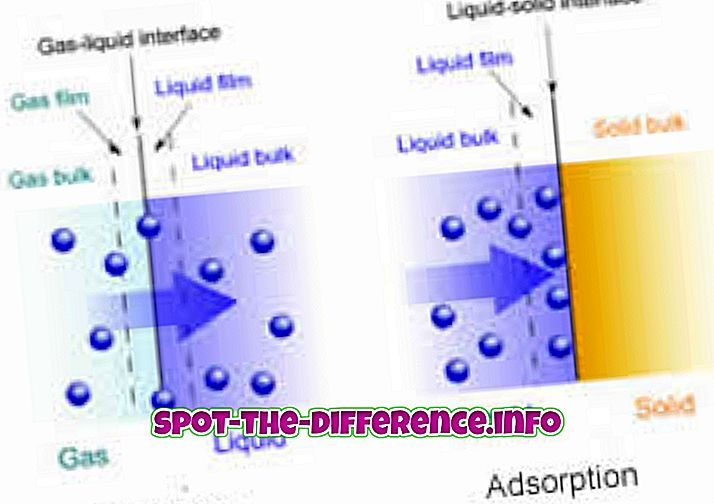
Chemická reakcia - oxid uhličitý absorbovaný roztokom uhličitanu draselného
Fyzikálny proces - vzduch absorbovaný vo vode rozpustením

Existujú dva typy režimov adsorpcie - chemické a fyzikálne. Pri chemickej adsorpcii sú molekuly a povrchy spojené slabými silami Vander Walls. Na druhej strane, pri chemickej adsorpcii sa medzi molekulami a povrchom vytvára chemická väzba.
Preto primárny rozdiel medzi adsorpciou a absorpciou spočíva v tom, že absorpcia je hromadný fenomén, čo znamená, že sa to deje v celom tele materiálu, zatiaľ čo adsorpcia zostáva povrchovým javom. Adsorpcia je vždy exotermická, zatiaľ čo absorpcia je endotermická. Sorpcia zahŕňa oba procesy absorpcie a adsorpcie.
Porovnanie adsorpcie a absorpcie:
adsorpčné | vstrebávanie | |
defintion | Akumulácia plynu alebo kvapalnej látky na povrchu pevnej látky alebo kvapaliny | Difúzia látky do kvapaliny alebo tuhej látky za vzniku roztoku alebo zlúčeniny |
príklad | Inertné plyny sa adsorbujú na aktívnom uhlí. | Suchá huba absorbuje vodu |
Výmena tepla | Exotermická s výnimkou adsorpcie H2 na skle | endothermic |
Dosiahnutie rovnováhy | Porovnateľne rýchlejšie | Porovnateľne pomaly |
sústredenie | Koncentrácia na povrchu adsorbentu sa líši od koncentrácie vo veľkom množstve | Koncentrácia zostáva rovnaká v celom materiáli |
Miera výskytu | Pôvodne je rýchlo, ale neskôr jeho sadzba začne klesať | Prebieha pri jednotnej sadzbe |